Методическая разработка семинарского занятия Тема «Периодический закон и Периодическая система Д.И. Менделеева»
Чикалова Любовь Георгиевна,
преподаватель химии,
ГАПОУ ЛО «Тихвинский промышленно-технологический техникум им. Е.И. Лебедева»
г. Тихвин, Ленинградская область
Методическая разработка семинарского занятия
Тема «Периодический закон и Периодическая система
Д.И. Менделеева»
Цель занятия:
Предметно-дидактическая: формирование умения давать характеристику элемента по положению в Периодической системе Д.И. Менделеева.
Планируемые результаты занятия:
Обучающие:
знают физический смысл порядкового номера элемента, номера периода, номера группы в ПС; порядок заполнения электронами энергетических подуровней;
применяют свои знания для характеристики элемента по положению в ПС Д.И. Менделеева;
используют приемы самоконтроля.
Развивающие:
развитие умения сравнивать, анализировать; выделять главное;
развитие навыков коллективной и самостоятельной работы;
развитие умения устанавливать причинно-следственные связи; излагать свои мысли; способствовать мотивации.
Воспитательные:
формирование способности к самооценке;
формирование профессионально значимых качеств личности через учебную дисциплину (организованность, внимательность, такт, ответственность, аккуратность).
Тип занятия:
по ведущей дидактической цели: повторение изученного материала;
по характеру совместной деятельности: синтетический (КСО - коллективный способ обучения);
по ведущему методу обучения: проблемный.
Методы обучения:
основной: проблемный;
дополнительные: работа в парах сменного состава, беседа, объяснение, самостоятельная работа, практическая работа и др.
Внутридисциплинарные связи:
применяют теоретические знания на практике;
решают химические задачи на применение полученных знаний.
Междисциплинарные:
определяют область знаемого и незнаемого.
Личностные:
осознают роль химии в познании окружающего мира.
Средства обучения:
Раздаточные материалы с заданиями для совместной работы в парах сменного состава (приложение).
Мультимедийная техника.
Таблицы: «Периодическая система Д.И. Менделеева», «План характеристики элемента по положению в ПС Д.И. Менделеева», «Зависимость свойств соединений элементов от положения в ПС Д.И. Менделеева».
Информационные источники:
Для студентов:
Литература:
Габриелян, О.С. Химия / О.С. Габриелян, И.Г. Остроумов// - Москва: Издательский центр «Академия», 2013.
Internet-ресурсы:
ЭБС «Консультант студента»
Для преподавателя:
Пресс И.А. Строение вещества: Учеб. пособие. – СПб.: СЗТУ, 2004. - 151 с.
Ход занятия:
Этапы занятия | Методы обучения | Содержание деятельности | оценка/само-оценка | |
преподавателя | студентов | |||
1. Орга-низационный. Мотивация учебной деятельности | Устное сообщение. | Приветствует обучающихся, проверяет их готовность к занятию. Создает определенный психологический настрой. Отмечает присутствующих с целью разделения группы на 2 равные подгруппы. | Приветствуют преподавателя, проверяют свою готовность к занятию. | |
2. Формирование новых знаний, умений и навыков. 2.1.Актуализация опорных знаний, умений и навыков. | Проблем-ный. Беседа. Коллективный способ обучения - пары сменного состава | Сообщает тему занятия, цель и задачи занятия. Организует работу студентов по следующим вопросам: - В каком году был сформулирован ПЗ Д.И. Менделеевым? -Дайте формулировку закона, предложенную Д.И. Менделеевым. - Что собой представляет таблица Периодической системы? -Дайте современную формулировку ПЗ. -Почему Д.И. Менделеев не мог дать эту формулировку? - Да, действительно, каждое обозначение в ПС имеет свой физический смысл – повторение и обобщение этого материала – цель нашего следующего этапа. Организует работу обучающихся в парах сменного состава по обучающим карточкам. | Записывают тему занятия в тетрадь. Отвечают на вопросы преподавателя: - ПЗ был сформулирован 1 марта 1869г. -Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов. - Таблица Периодической системы – это графическое отображение ПЗ. -Свойства химических элементов и образуемых ими веществ находятся в периодической зависимости от величины заряда их атомных ядер. - Не было известно строение атома. Выполняют работу в парах сменного состава. | Самоконтроль и взаимоконтроль выполнения заданий каждой карточки. |
2.2. Создание проблемной ситуации. | Беседа. | Организует работу студентов по следующим вопросам: - Подумайте, в чем причина периодичности? Диктует вывод: «Свойства ХЭ и образованных ими веществ находятся в периодической зависимости от строения внешних электронных слоев атомов». - Подумайте, характеристики, каких химических понятий Вы изучали сейчас, при работе в парах? | Анализируют, обсуждают ответы друг друга, приходят к выводу о том, что причина периодичности свойств элементов заключается в периодической повторяемости сходных электронных конфигураций (строения наружного энергетического уровня). Записывают вывод: «Свойства ХЭ и образованных ими веществ находятся в периодической зависимости от строения внешних электронных слоев атомов» Анализируют, обсуждают ответы друг друга, приходят к выводу о том, что изучали характеристики атома химического элемента, изменение свойств по периоду и группе, характер свойств высшего оксида, высшего гидроксида, образованных данным химическим элементом. | Совместное обсуждение. |
2.3.Постановка учебной проблемы. | - Составьте план, по которому можно дать характеристику атома химического элемента по положению в ПС Д.И. Менделеева? | Воспринимают учебную проблему. | ||
2.4. Решение учебной проблемы. а) выдвижение гипотезы; б) проверка гипотезы и формулировка окончательного решения. | Самостоятельная работа, работа в парах. Самостоятельная работа | Организует деятельность обучающихся по решению учебной проблемы: 1.Составление плана решения поставленной задачи. 2. Решение задачи. 3.Формулировка гипотезы в виде вывода по итогам решения задачи. Сопровождает обучающихся в процессе решения задачи и выдвижения гипотезы. Организует работу по проверке выдвинутой гипотезы, подтверждает верность высказанного предположения; выдает эталон на бумажном носителе. | Формулируют гипотезу на основе анализа характеристики атома химического элемента, изменения свойств химического элемента по периоду и группе, характера свойств высшего оксида, высшего гидроксида, образованных данным химическим элементом. Предлагают свой план характеристики химического элемента по положению в ПС. | Совместное обсуждение. Самопроверка, сравнение с эталоном (раздаточный материал). |
2.5. Доказатель-ство и применение найденного решения. | Самостоятельная работа Проверочная работа | Организует деятельность обучающихся по работе о характеристике элемента хлора по положению в ПСХЭ в соответствии с планом. Организует деятельность обучающихся по решению задачи – характеристика калия по положению в ПСХЭ. | Выполняют по плану характеристику элемента хлора по положению в ПХЭ. Выполняют задание в соответствии с предложенным планом и сдают выполненное задание на проверку преподавателю. | Совместное обсуждение, сравнение с эталоном (характеристика хлора). Оценка преподавателем. |
3. Информация о д/з, инструктаж по его выполнению, рефлексия, подведение итогов | Беседа. | Организует деятельность по записи д/з: дать характеристику элемента алюминия по положению в ПСХЭ, анализу работы на занятии, благодарит за работу: -Пожалуйста, на маленьких листочках ответьте на любой из предложенных вопросов (можно на все):
Приводит слова Д.И. Менделеева "По видимости, периодическому закону будущее не грозит разрушением, а только надстройки и развитие обещает» Д. И. Менделеев - Спасибо за работу! | Делают запись д/з, письменно отвечают на вопросы, анализируют, делают выводы. | Совместное обсуждение. |
Приложение
«Раздаточный материал»
Строение атома
Атом - химически неделимая нейтральная частица.
Атом - сложная частица: в центре атома находится положительно заряженное ядро, состоящее из элементарных частиц – протонов (¦р), нейтронов (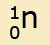 ), вокруг ядра вращаются электроны ( e−).
), вокруг ядра вращаются электроны ( e−).
Электроны – (-) заряженные частицы.
Протоны – (+) заряженные частицы.
Нейтроны – не имеют заряда.
Физический смысл порядкового номера элемента - N (элемента) показывает (равен) = положительный заряд ядра атома элемента = число протонов (¦р) в ядре = число всех электронов ( e−).
Число нейтронов (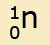 ) = Ar (элемента)-N(элемента)
) = Ar (элемента)-N(элемента)
Электроны в атоме расположены не хаотично, а упорядоченно - слоями. Слой e− называют энергетический уровень.
Электроны, расположенные на последнем энергетическом уровне называют внешние (валентные электроны). Чаще всего, в образовании химических связей участвуют внешние электроны.
Физический смысл номера периода - показывает количество энергетических уровней.
Период – это горизонтальный ряд Периодической системы, который начинается щелочным металлом и заканчивается инертным газом.
Различают периоды:
малые (состоят из одного ряда)
большие (состоят из двух рядов)
Физический смысл номера группы - показывает количество внешних (валентных e−) для элементов главных подгрупп.
Группа – это вертикальный ряд Периодической системы (8 групп).
В каждой группе различают:
элементы главной подгруппы (А) (sиp)
элементы побочной подгруппы (В) (d и f)
Главная подгруппа начинается с элементов малых периодов.
Элементы главных подгрупп - (s,p) – элементы (имеют s,p–электроны наружного энергетического уровня).
Элементы побочных подгрупп - (d,f) – элементы (имеют d,f – электроны внутренних энергетических уровней).
Пример: определите состав атома магния. Решение: порядковый номер атома магния = 12. Следовательно, заряд ядра =+12; число протонов = 12; число всех электронов = 12. Относительная атомная масса = 24; следовательно, число нейтронов = 24-12 = 12. Номер периода «3», следовательно, число энергетических уровней = 3. Номер группы «2», следовательно, число внешних (валентных) электронов = 2.
Задание (выполните в тетради письменно): определите состав атома фосфора.
Электронные и графические схемы
Порядок заполнения электронами энергетических подуровней происходит в соответствии с правилами Клечковского:
1 правило - «Электроны в пределах одного энергетического уровня заполняют тот подуровень, для которого сумма (n+l) минимальна».
2 правило - «В случае, когда сумма (n+l) одинакова, заполняется подуровень с меньшим значением n».
Из правил Клечковского следует Порядок заполнения электронами энергетических подуровней.
Порядок заполнения электронами энергетических подуровней.
1s2s2p3s3p4s3d4p5s4d5p6s5d14f5d6p7s6d15f6d7p
5d1-учитывать только для лантаноидов (Э (N) 58-71)
6d1-учитывать только для актиноидов (Э (N) 90-103)
Пользуясь этим порядком, составляют электронные (и графические) схемы строения атомов.
Помнить!
s – подуровень (1 орбиталь) максимально может находиться 2 e−
p – подуровень (3 орбитали) максимально может находиться 6 e−
d – подуровень (5 орбиталей) максимально может находиться 10 e−
f – подуровень (7 орбиталей) максимально может находиться 14 e−
Электроны заполняют подуровни максимально, затем – по остаточному принципу.
Электронная конфигурация (электронная формула) дает возможность определить принадлежность химического элемента к семейству (s,p,d,f): какой энергетический подуровень заполняется последним, такой и элемент.
Правило Гунда (Хунда)
«Электроны в пределах одного энергетического подуровня располагаются таким образом, чтобы их суммарный спин был максимальным».
Электроны с антипараллельными спинами спариваются.
Пример: составьте электронную схему строения атома фосфора. Решение: N(P) = 15 электронная схема 1s22s22p63s23p3, строение наружного энергетического уровня 3s23p3, графическая схема строения наружного энергетического уровня
Фосфор – р-элемент.
Задание (выполните в тетради письменно): составьте электронную схему строения атома магния.
Классификация элементов
Химические элементы можно классифицировать не только по характеру застройки их электронных конфигураций, но и по их свойствам. Классификация химических элементов по свойствам подразумевает их деление на:
Металлы – элементы главных подгрупп с числом валентных электронов от1 до3 (подгруппы IA, IIA, IIIA, кроме элемента бора), а также германий, олово, свинец, сурьма, висмут и полоний;
неметаллы – бор и элементы главных подгрупп с числом валентных электронов от4 до7 (подгруппы IVA, VA, VIA, VIIA) кроме германия, олова, свинца, сурьмы, висмута и полония;
переходные элементы– элементы побочных подгрупп (IB–VIIB); в виде простых веществ ведут себя как металлы;
благородные газы – элементы подгруппы VIIIA, атомы которых отличаются наиболее стабильными электронными конфигурациями (полностью завершенные энергетические подуровни).
Пример: проклассифицируйте следующие элементы по свойствам: магний, фосфор, самарий, ксенон, фтор. Решение: магний (IIA), фосфор (VA), самарий (IIIB), ксенон (VIIIA), фтор (VIIA). Следовательно, металл – магний; неметалл – фосфор, фтор; переходный элемент – самарий; благородный газ – ксенон.
Задание (выполните в тетради письменно): проклассифицируйте следующие элементы по свойствам: сера, азот, рубидий, гелий.
Изменение металлических и восстановительных свойств
Металлические свойства (восстановительные свойства) – способность атома (простого вещества) отдавать электроны.
Под металлическими (или восстановительными) свойствами элементов понимают способность их атомов к отдаче валентных электронов.
Металлические свойства наиболее характерны для элементов, атомы которых имеют небольшое число электронов на внешнем энергетическом уровне.
По периоду (горизонтальный ряд ПС) металлические (восстановительные) свойства уменьшаются, т.к. возрастает заряд ядра атомов элементов и уменьшается радиус атомов элементов.
По группе (вертикальный ряд) металлические (восстановительные) свойства возрастают, т.к. возрастает радиус атомов элементов.
Пример: расположите элементы: бериллий, углерод, литий в порядке увеличения металлических свойств. Решение: элементы находятся в одном периоде; по периоду металлические свойства уменьшаются, следовательно, углерод проявляет наименьшие металлические свойства, а литий – наибольшие. Ряд: углерод, бериллий, литий.
Задание (выполните в тетради письменно): расположите элементы: стронций, бериллий, магний в порядке возрастания металлических свойств.
Изменение неметаллических и окислительных свойств
Неметаллические свойства (окислительная активность) – способность атомов элементов к присоединению электронов.
Неметаллические свойства (окислительные свойства) – способность атома (простого вещества) принимать электроны.
Движущей силой этого процесса является стремление атомов приобрести наиболее стабильную восьмиэлектронную конфигурацию благородных газов. Наибольшую тенденцию к присоединению электронов имеют атомы p-элементов, обладающие относительно большим числом собственных валентных электронов.
Количественной характеристикой неметаллических свойств (мерой неметаллических свойств) является электроотрицательность (ЭО; Х)
ЭО – способность атома принимать на себя электроны (см. последний форзац учебника – ряд «Электроотрицательность»).
По периоду (горизонтальный ряд ПС) неметаллические (окислительные) свойства увеличиваются, т.к. возрастает заряд ядра атомов элементов и уменьшается радиус атомов элементов.
По группе (вертикальный ряд ПС) неметаллические (окислительные) свойства уменьшаются, т.к. возрастает радиус атомов элементов.
Пример: расположите элементы: сера, селен, кислород в порядке увеличения неметаллических свойств. Решение: элементы находятся в одной группе; по группе неметаллические свойства уменьшаются, следовательно, селен проявляет наименьшие неметаллические свойства, а кислород – наибольшие. Ряд: кислород, сера, селен.
Задание (выполните в тетради письменно): расположите элементы: алюминий, магний, кремний в порядке возрастания неметаллических свойств.
Изменение основных и кислотных свойств
Основные свойства – это способность соединения элемента (высшего оксида, высшего гидроксида) взаимодействовать с кислотами.
Кислотные свойства - это способность соединения элемента (высшего оксида, высшего гидроксида) взаимодействовать с основаниями.
По периоду (горизонтальный ряд ПС) основные свойства (ВО, ВГ) уменьшаются, кислотные свойства (ВО, ВГ) увеличиваются, т.к. возрастает заряд ядра атомов элементов и уменьшается радиус атомов элементов.
По группе (вертикальный ряд ПС) основные свойства (ВО, ВГ) увеличиваются, кислотные свойства (ВО, ВГ) уменьшаются, т.к. возрастает радиус атомов элементов.
Пример: определите характер высших оксидов:Li2O,SiO2,SrO. Решение: Li (IA), следовательно, Li2O – основный; Si (IVA), следовательно, SiO2- кислотный , Sr (IIA), следовательно, SrO – основный (смотри таблицу «Формулы высших оксидов, высших гидроксидов и их характер в зависимости от положения в ПС Д.И. Менделеева»).
Задание (выполните в тетради письменно): определите характер высших гидроксидов: брома, углерода, кальция.
Формулы высших оксидов, высших гидроксидов и их характер
в зависимости от положения элемента в Периодической системе Д. И. Менделеева
Номер группы | Электронные формулы строения наружного энергетического уровня | Формула высшего оксида, характер | Формула высшего гидроксида, характер |
I (A) | ns1 | R2O (основный) | ROH(основный) |
II (A) | ns2 | RO(основный)BeO(амфотерный) | R(OH)2 (основный) Be(OH)2 (амфотерный) |
III (A) | ns2np1 | R2O3 (амфотерный) B2O3 (кислотный) | R(OH)3 (амфотерный) HBO2 (кислота) |
IV (A) | ns2np2 | RO2(кислотный) | H2RO3 (кислота) |
V (A) | ns2np3 | R2O5 (кислотный) | H3RO4 (кислота), но HNO3 |
VI(A) | ns2np4 | RO3 (кислотный) | H2RO4 (кислота) |
VII (A) | ns2np5 | R2O7 (кислотный), иск.F | HRO4 (кислота), искл.F |
План характеристики элемента по положению в Периодической системе Д.И. Менделеева.
Строение атома
Номер элемента N (эл.)=
заряд ядра атома +q =
число протонов (¦Р)=
число электронов (e−)=
Относительная атомная масса химического элемента (Ar)=
число нейтронов (
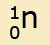 )=Ar(эл.)-N (эл.)=
)=Ar(эл.)-N (эл.)=N периода = ; число энергетических уровней =
N группы = ; число внешних (валентных) электронов =
Электронная схема строения атома.
Строение наружного энергетического уровня.
Графическая схема строения наружного энергетического уровня атома
Качество элемента (s,p,d,f)
Свойства элемента (металлические или неметаллические)
Сравнение свойств по периоду
Сравнение свойств по группе
Свойства соединений
Формула высшего оксида (ВО), его характер;
Формула высшего гидроксида (ВГ), его характер;
Формула летучего водородного соединения (ЛВС) (если есть).
Характеристика элемента хлора по положению в Периодической системе Д.И. Менделеева (эталон ответа)
I. Строение атома хлора (Cl)
Номер элемента N(Cl)=17
заряд ядра атома +q =+17
число протонов (¦Р)=17
число электронов (e−)=17
относительная атомная масса химического элемента Ar (Cl)=35
число нейтронов (
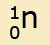 )=Ar(Cl)-N (Cl)=35-17=18
)=Ar(Cl)-N (Cl)=35-17=18N периода = 3; число энергетических уровней = 3
N группы = 7; число внешних (валентных) электронов =7
Электронная схема строения атома 1s22s22p63s23p5
Строение наружного энергетического уровня 3s23p5
Графическая схема строения наружного энергетического уровня
Качество элемента: p - элемент
II. Свойства элемента хлора: Cl проявляет неметаллические свойства
Сравнение неметаллических свойств по периоду: S < Cl < Ar ( возрастают), т.к. уменьшается радиус атомов элементов, увеличивается заряд ядра атомов.
Сравнение неметаллических свойств по группе: F > Cl > Br (убывают), т.к. увеличивается радиус атомов элементов.
III.Свойства соединений
Формула высшего оксида (ВО) - Cl2О7, его характер - кислотный;
Формула высшего гидроксида (ВГ) - НClО4, его характер – кислотный (кислота);
Формула летучего водородного соединения (ЛВС) - НCl (хлороводород)

 Приказ о проведении
Приказ о проведении
 Положение
Положение
 Выписка из Протокола
Выписка из Протокола
 Диплом победителя
Диплом победителя
 Диплом за инновационную деятельность
Диплом за инновационную деятельность
 Благодарность
Благодарность
























































Чтобы оставлять комментарии, вам необходимо авторизоваться на сайте. Если у вас еще нет учетной записи на нашем сайте, предлагаем зарегистрироваться. Это займет не более 5 минут.