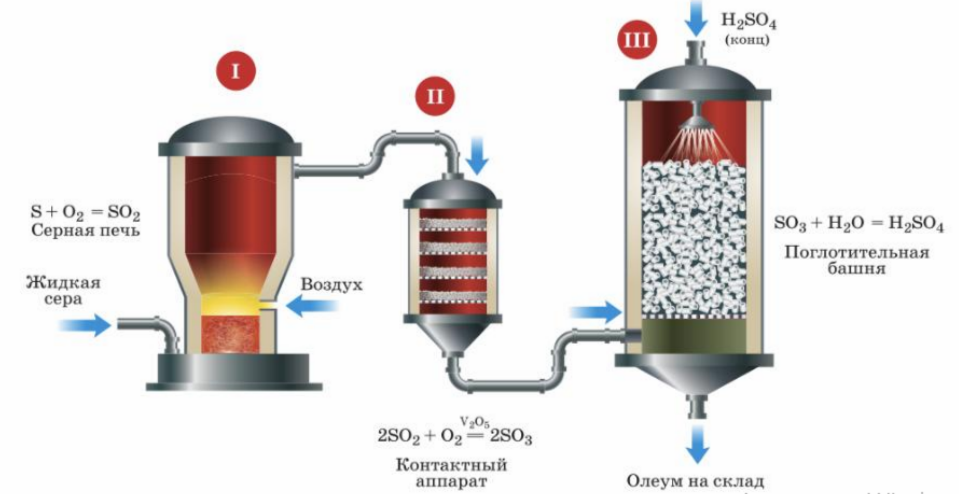
Мне не раз доводилось встречать разнообразные схемы-иллюстрации промышленного производства H₂SO₄ (контактным методом). К сожалению, я не видела ни одной схемы без этой, на мой взгляд, грубейшей ошибки. Ниже представлена достаточно упрощенная схема данного процесса (и снова не без ошибки).
Именно поэтому так важно развивать у учащихся критическое мышление. Предлагаю вам обсудить на уроке процесс производства серной кислоты, разобрав поэтапно, что происходит от попадания сырья в печь для обжига и до получения конечного продукта, и сопоставить процесс со схемой. Особое внимание следует уделить конечному процессу, происходящему в поглотительной башне (III): ни в коем случае нельзя проводить гидратацию SO₃, как показано в уравнении на схеме, ввиду выделения огромного количества тепла. Вода вскипает мгновенно, образуется пар, который реагирует с SO₃ и образует «сернокислотный туман», который далее с потоком пара уносится в атмосферу, что может привести к катастрофическим последствиям!
Следует сделать акцент на этом и снова вернуться к рисунку. На той же схеме над поглотительной башней верно показано, что орошение ведется концентрированной серной кислотой, при этом на выходе образуется олеум:
H₂SO₄ (конц.) + nSO₃ = H₂SO₄ · nSO₃ (олеум)
Обсуждение этой детали на уроке поможет учащимся не просто запомнить схему, а понять значение точности в химических процессах и опасность поверхностного восприятия информации.








































Чтобы оставлять комментарии, вам необходимо авторизоваться на сайте. Если у вас еще нет учетной записи на нашем сайте, предлагаем зарегистрироваться. Это займет не более 5 минут.