Водород как химический элемент и простое вещество. Получение водорода в лаборатории. Реакция замещения
Тема урока:Водород как химический элемент и простое вещество. Получение водорода в лаборатории.Реакция замещения
Цели урока: ознакомить учащихся с историей открытия водорода; его распространением в природе; конкретизировать знания обучающихся о водороде как элементе и простом веществе, сформировать понятия о реакциях замещения и сравнение их с реакциями разложения и соединения; выучить меры безопасности во время работы с водородом.
Задачи:
образовательная: обеспечить усвоение учащимися понятий: “водород – химический элемент”, “водород – простое вещество”, познакомить нахождением водорода в природе, с физическими свойствами водорода, методами получения водорода в промышленности и в лаборатории и способами его собирания.
развивающая: развитие умений учебного труда; развитие умения строить заключения на основе наблюдения; развитие познавательных умений; формирование научного мировоззрения, развитие логического мышления.
воспитательная: воспитание мотивов учения, положительного отношения к занятиям, умению рефлексировать, стремление добиваться наилучших результатов, воспитание дисциплинированности.
Тип урока: изучение нового материала.
Формы и методы работы: групповая работа, фронтальная работа, игра «кроссворд», «микрофон»
Оборудование:Периодическая система химических элементов
Д.И.Менделеева, штатив с пробирками, аппарат Киппа,раствор соляной кислоты, Mg,Zn,Fe, прибор для получения газов, спички.
Ориентировочный план и методы проведения урока
1. Объявление темы и предполагаемых результатов урока - 3-5 мин.
Изучение темы (ажурная пилка)- 30-35 мин.
Оценивание результатов урока учащимися (микрофон) - 5-7 мин.
Предполагаемые результаты
Учащиеся должны выяснить:
открытие водорода;
распространение водорода в природе;
физические свойства водорода;
получение Н2 в лаборатории;
реакция замещения.
Организация деятельности учащихся
Игра(кроссворд - 7 вопросов).
Свойство атомов химического элемента соединяться с
определенным числом атомов других элементов.Вещества, которые изменяют скорость реакции, но не входят в
состав продуктов.Как называются реакции, в результате которой из нескольких
веществ образуется одно сложное.Сложные вещества, образованные двумя элементами, один из
которых кислород.Условное изображение с помощью химических формул.
Мельчайшая частица химического элемента.
Число, показывающее количество атомов химического элемента вформуле - ?
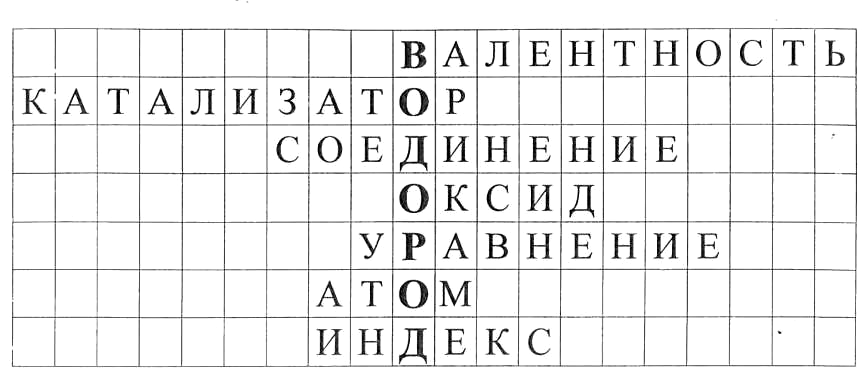
В результате разгадывания объявляется темаурока "Водород» и предполагаемые результаты урока
2.Интерактивная часть. Изучение темы «Водород» (ажурная пилка).
Iэтап. Учащиеся объединяются в 4 группы и каждая группа
получает задание.
IIэтап.Составляется «экспертная группа» (остальные учащиеся в
группах получают индивидуальные задания).
IIIэтап. Эксперты возвращаются в свои рабочие группы,
обрабатывают полученную информацию в полном объеме,анализируют материалы в целом.
Физкультминутка.
Для закрепления выступают эксперты с обобщенным материалом по своему вопросу.
Проводится демонстрация получения Н2 в лаборатории (учитель). Записываются уравнения реакции:
Zn + НС1→
Mg + НС1→
Fe + НС1→
Рассматривается реакция замещения (учитель + учебник + ученик).
IVэтап.Оценивание результатов урока (микрофон):
достигли ли желаемых результатов на уроке?
над чем еще надо работать?
Домашнее задание: § 24 (повторить § 20), задание 7 стр.84.
ПРИЛОЖЕНИЕ 1
1. Задание для группы
Прочесть пункт «Физические свойства водорода» по учебнику стр. 82 и ответить навопросы:
как можно собрать водород?
в чем различие по сравнению со способом сбора кислорода?
2. Индивидуальные задания
Решите задачу:Вычислите массовую долю элемента водорода в соединениях: Н2О,НСl.
Решите задачу:Вычислите массовую долю элемента водорода в соединениях: H2SO4, РН3 .
Решите задачу:
Вычислите массовую долю элемента водорода в соединениях: HNO3, СН4
Решите задачу:
Вычислите массовую долю элемента водорода в соединениях Н2СО3 , NH3.
ПРИЛОЖЕНИЕ 2
ИСТОРИЯ ОТКРЫТИЯ ВОДОРОДА.
Водород впервые открыл английский ученый Генри Кавендиш. Кавендиш получил водород при помощи взаимодействия цинка, олова или железа с серной или соляной кислотами.
Водород описывали до Кавендиша и другиеисследователи, принимая его за разновидность воздуха или флогистон, однако они не пыталисьизучить его свойства. В1660г. Р. Бойль получилводород, действуя соляной кислотой на железные стружки, и охарактеризовал его как«воздух, рожденный или произведенный заново». В 1745г. о водороде писал М.В. Ломоносов: «При растворении какого-либо неблагородного металла, особенно железа, в кислотных спиртах из отверстия склянки вырывается «горючий пар».
Кавендиш впервые подробно описывал способы получения и специфические признакиводорода.
По предложению французского физика ихимика А. Гитона де Морво в 1787г. вместо «горючего воздуха» было введено латинскогоназвания «гидрогениум» (от греч. «гидро» и«геннао»), означающее «рождающий воду».
Водород стал первым известным газообразным веществом элементарной природы, и его открытие имело огромное значение для современной химии.
ВОДОРОД В ПРИРОДЕ.
Из-за высокой химической активности водородвстречается на Земле в виде соединений с другими элементами. Так, в воде, самом распространенном на Земле веществе, массовая доля водорода составляет11,19%. Содержание водорода в земной коресоставляет около 1% по массе и 17% от общего числаатомов. Он входит в состав многих минералов игорных пород, а также всех органических соединений. Водород - важная составная часть кислот, многие из которых содержатся в растениях и животных. Онвходит в состав компонентов природного газа и нефти. Незначительное количество газообразноговодорода находится в вулканических газах. Верхниеслои атмосферы на 80-90 % состоят из водорода.
Водород - самый распространенный элемент воВселенной. Он составляет около половины массыСолнца и большинства звезд. Из водорода состоятгазы межзвездной среды и газовые туманности,причем в составе межзвездной среды и туманностейводород находится не в виде молекулы Н2 , а в виде отдельных атомов (атомарный водород). Для образования молекулы необходимо, чтобы два атомаводорода столкнулись друг с другом, но в космическом пространстве концентрация веществнастолько низка (в межзвездной среде - примерноодин атом водорода на 1 см пространства,туманностях - около 100 атомов на 1 см), что атомыводорода двигаются свободно, не сталкиваясь друг с другом.


 Приказ о проведении
Приказ о проведении
 Положение
Положение
 Выписка из Протокола
Выписка из Протокола
 Диплом победителя
Диплом победителя
 Диплом за инновационную деятельность
Диплом за инновационную деятельность
 Благодарность
Благодарность




















































Чтобы оставлять комментарии, вам необходимо авторизоваться на сайте. Если у вас еще нет учетной записи на нашем сайте, предлагаем зарегистрироваться. Это займет не более 5 минут.