урок химии по теме "Вода. Растворы. Растворение"
| Автономное учреждение профессионального образования Ханты – Мансийского автономного округа - Югры |
«СУРГУТСКИЙ ПОЛИТЕХНИЧЕСКИЙ КОЛЛЕДЖ» |
Методическая разработка
открытого урока по химии
Тема: «Вода. Растворы. Растворение».

Должность | Фамилия/ подпись | Дата | |
Разработал | Штыхлина И.В. | 26.03.2018 | |
Проверил | Масанина Т.Н. | 26.03.2018 | |
Согласовал | Масанина Т.Н. | 26.03.2018 |
Штыхлина Ирина Васильевна,
преподаватель химии СПК СП-1
1 курс группа 702
«Строительство и эксплуатация зданий и сооружений»
В разделе «Вода. Растворы. Электролитическая диссоциация» - это первый урок.
Тема: Вода. Растворы. Растворение.
Цель: Познакомиться с растворами.
Задачи:
изучить свойства воды, как растворителя;
узнать виды растворов;
научиться решать задачи с использованием понятия массовая доля растворенного вещества;
Методы: урок проблемного обучения
Технологии: технология критического мышления, дискуссионная, коллективная и индивидуальная, мыслительная деятельность.
Планируемые результаты:
знать основные понятия урока.
уметь решать расчетные задачи с использованием понятия «Массовая доля растворенного вещества в растворе».
Техническое обеспечение урока: компьютер, медиапроектор, экран.
Методическое и дидактическое обеспечение урока: презентация, учебник, раздаточный материал.
Структура урока:
Организационный момент (2 мин).
Актуализация опорных знаний (10 мин).
учебный фильм;
домашнее задание.
Основная часть урока (40 мин):
классификация дисперсных систем и растворов;
способы выражения концентрации вещества в растворе;
решение расчетных задач с использованием понятия «Массовая
доля растворенного вещества в растворе».
Закрепление изученного материала (20 мин):
решение задач (работа в группах).
Итоги урока (5 мин)
выставление отметок
Рефлексия. (3 мин)
Резерв:высказывания ученых
Ход урока:
1. Орг. момент, создание психологического настроя на работу.
Доброе утро, ребята! Я рада вас видеть и надеюсь, что мы с вами сегодня проведем вместе хороший, интересный урок.
2. Актуализация знаний.
- Посмотрите короткий фрагмент документального фильма: что вы увидели? (море, вода и т.п.)
- Теперь я предлагаю вам посмотреть на море глазами химика – чем является морская вода? (смесью, раствором солей и т.п.)
- Молодцы, вы практически назвали тему урока, осталось сформулировать вопросы, которые нам предстоит рассмотреть.
-Как вам кажется, о чем сегодня стоит поговорить на уроке? (что такое растворы, какие они бывают, где применяются, как готовятся и т.д.)
-Вот вы и сформулировали задачи, стоящие перед нами. Давайте откроем тетради, запишем число и тему урока: «Вода. Растворы. Растворение».(Слайд 1, 2)
Цель: познакомиться с растворами
Задачи:
Изучить свойства воды, как растворителя
Знать виды растворов
Научиться решать задачи с использованием понятия массовая доля растворенного вещества.
- Запишем домашнее задание: изучить п. 11, 12; письменно ответить на вопросы 3, 4, 5, 6, стр. 104; решить задачи 6, 7, 12 на стр. 111(Слайд 3)
- Тема «Вода» вами рассматривалась на уроках географии, физики, биологии и химии в младших классах.
- Что вы помните из школьного курса о воде? (учащиеся дают ответы) (Слайд 4)
«Вода, у тебя нет ни вкуса, ни цвета, ни запаха, тебя невозможно описать, тобой наслаждаются, не ведая, что ты такое. Нельзя сказать, что ты необходима для жизни: ты — сама жизнь. Ты наполняешь нас радостью, которую не объяснить нашими чувствами». Антуан де Сент-Экзюпери
Применение воды очень огромное и свойств у воды много.
Одной из ее главных особенностей является способность растворять различные вещества: и газы, и жидкости, и, конечно, твёрдые вещества. (Слайд 5, 6)
- Что такое раствор? Что такое растворитель? Что такое растворенное вещество? На эти и другие вопросы мы сегодня с вами ответим. Давайте посмотрим опыты.
3. Основная часть урока:
ОПЫТ. (проводит преподаватель вместе с помощником)
На столе стаканы с водой:
1-ый стакан: вода + масло (Эмульсия - это система, в которой частицы одной жидкости распределены в другой жидкости)
2-й стакан: вода + мел (Суспензия – это система, в которой частицы твердого вещества распределены в жидкости)
3-й стакан: вода + соль
4-й стакан: гидроксид натрия и вода.
- Что общего и чем отличаются эти опыты?(Слайд 7)
Сходство: смешивали вещества, присутствует вода и т.д.
Отличие: в 1 и во 2 стаканах вещества видны невооруженным глазом, они не растворяются; в 3 стакане вещество растворилось и мы его не видим, а в 4-м – раствор нагрелся.
Вывод: в 1-м случае вещества не растворяются, но смешиваются, образуя неоднородную смесь – дисперсную систему, во 2-м случае вещества растворились и образовали однородную смесь, которая называется – истинным раствором, в 3 – образовалось новое вещество.
- Д.И. Менделеев изучая растворы делает вывод: Растворение – это физико-химический процесс (делают записи в тетрадях).
- Перед вами на столе находится коллекция дисперсных систем, мне бы хотелось чтобы вы, используя учебник на стр. 96-102, попытались классифицировать эти системы на группы (ребята пытаются выполнить задание). (работа в группах).
Каждой группе предложено определить дисперсную систему и ответить на вопрос, консультанты являются помощниками и в конце работы оценивает каждого учащегося.
1-я группа: молоко, нефть, капельки жира в лимфе.
ВОПРОС: Дайте определение эмульсий и приведите примеры эмульсий, которые человек применяет в практической деятельности?
2- я группа: зубная паста, мази.
ВОПРОС: Дайте определение суспензий и назовите практически значимые строительные суспензии?
3-я группа: гели для душа, почва, гели после бритья, кремы.
ВОПРОС: Чем определяется срок годности косметических и медицинских гелей?
- Для человека и животных этот процесс (синерезис) (Слайд 8) очень важен т.к. сопровождает свертывание крови. Если этот процесс затруднен, то это указывает на наличие у человека заболевания – гемофилии. Из курса биологии вам известно, носители гемофилии женщины, а заболевают мужчины. Какой исторический пример вам известен?
4-я группа. Как классифицируют дисперсные систем по агрегатному состоянию дисперсионной среды и дисперсной фазы? Приведите примеры, используя рис. 88 стр. 104 (Слайд 9, 10, 11).
- Посмотрите внимательно вокруг себя. Туман, пыль, снег, ткани живых организмов, земная кора, космическое пространство часто представляют собой примеры дисперсных систем.Мы живем в мире дисперсных систем.
- А сейчас мы вернемся к нашему опыту, в 3-м и 4-м стаканах мы с вами видели, что вещества полностью растворились и образовали истинный раствор.
- Что же такое раствор? Попробуйте самостоятельно сформулировать определение. (записывают в тетрадях). Прочитайте, что у вас получилось?
Раство́р — гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия. (Слайд 12,13) (определение)
- Теперь мы с вами знаем, что одни вещества растворяются, а другие образуют дисперсные системы.
- В зависимости от количества растворенного вещества, растворы бывают: ненасыщенные,
насыщенные, перенасыщенные. Классификация (Слайд 14) (привести пример с чаем и сахаром, соленые озера)
-Все знают об уникальных свойствах Мёртвого моря. Но и в России есть немало солёных озер, химический состав которых похож с Мёртвым морем, и оказывает целебное влияние на человеческий организм.
Наши предки наделяли соль особыми качествами. Считалось, что она имеет энергетику, влияющую на здоровье человека. Говорят, что разработку соляных озёр в России начал император Александр III. По легенде, попав в железнодорожную катастрофу, он сумел поправить свое здоровье благодаря соленой воде из Оренбургской области. Так появился первый соляной курорт в Соль-Илецке. С 19 века началось активное развитие новых целебных озер по всей территории России.
- Как мы уже выяснили, область применения весьма обширна, поэтому очень важно в разных областях: медицине, с\х, а в быту вам приходилось приготавливать растворы.
Как это нужно делать правильно?
- Для выражения количественного состава раствора используется понятие массовой доли растворенного вещества.Это отношение растворенного вещества к суммарной массе раствора.
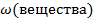 =
=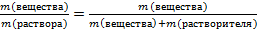 (Слайд 15)
(Слайд 15)
- Рассмотрим несколько задач.
Обучающиеся под руководством преподавателя решают расчетные задачи разных типов.
Задача №1. Вычислить массовую долю растворенного вещества, если масса раствора 500 г, а масса соли 25 г. Ответ 5%
Задача №2. В воде массой 40 г растворили 10 г сахара. Определить массовую долю раствора.Ответ 20%
Задача №3. Для полоскания горла используют 4% раствор пищевой соды. Сколько понадобиться соды и воды, что бы приготовить раствор массой 200 г?
Ответ соды -8 г, воды- 192 г
Задача №4. Рассчитать массу воды, которую необходимо добавить к раствору гидроксида калия массой 200 г с массовой долей растворенного вещества 12% для приготовления раствора с массовой долей 5% гидроксида калия?Ответ соли - 24 г, воды – 280 г
4. Закрепление изученного материала
В качестве закрепления изученного материала обучающимся предлагается самостоятельно решить задачи:
1 группа.«Фармацевты» Заменителем крови является 0,9% раствор поваренной соли. Рассчитайте сколько необходимо взять соли и воды, для приготовления 100 г такого раствора?Ответ 0,9 г соли, 99,1 г воды
2 группа. «Лаборанты» На урок химии лаборанту для опытов необходимо приготовить раствор серной кислоты. Рассчитайте массу воды, которую необходимо добавить к раствору серной кислоты, массой 100 г с массовой долей вещества 70% для приготовления раствора с массовой долей 9%? Ответ 677 г
3 группа.«Домохозяйки» Соление огурцов производят в 5%-ном растворе поваренной соли. Сколько соли и воды необходимо для приготовления 500 г такого раствора? Ответ 25 г соли 475 г воды
4 группа. «Строители» Чтобы построить современный долговечный дом − обойтись без раствора, практически, невозможно. Он нужен для устройства фундамента, полов, кладки стен, монтажа плит перекрытия, возведения камина и внутренней отделки помещений и фасада дома. Это далеко не полный перечень работ, где может применяться тот или иной вид строительного раствора.
Задача. Необходимо приготовить 15% известковый раствор массой 140 г, сколько вы возьмете воды и сколько оксида кальция для приготовления раствора? Ответ 21 г соли, 119 г воды
По окончанию работы 1 студент с группы записывает решение задачи на доске. Другие учащиеся дают устный ответ (опережающее домашнее задание «Применение растворов»).
Учащиеся других групп внимательно слушают и готовят вопросы для докладчика
5. Рефлексия. Итоги урока.
Ребята, давайте мы с вами мысленно вернемся к началу урока и вспомним, какие цели и задачи мы ставили перед собой? Достигли ли мы их? Что не вызвало затруднений, с какими трудностями столкнулись? Насколько вы довольны своей работой?
На партах листочки с рефлексией, ребятам необходимо продолжить
Что было трудным на уроке?
Что понравилось?
Что узнали нового о растворах?
Чему удивились?
Резерв времени: У вас на столах слова великих людей, прочитайте и скажите как вы их понимаете?
1 группа.«Вода стоит особняком в истории нашей планеты. Нет природного тела, которое могло бы с ней сравниться по влиянию на ход основных, самых грандиозных, геологических процессов».Владимир Иванович Вернадский
2 группа. «Вода – красота всей природы. Вода жива, она бежит или волнуется ветром, она движется и дает жизнь и движение всему ее окружающему». Сергей Аксаков
3 группа. «Она есть повсюду; она соприкасается с прошлым и готовит будущее; она струится под полюсами и присутствует на больших высотах. Если есть что-то поистине загадочное на этой планете, так это вода».Лорен Эйсли
4 группа. «Воде была дана волшебная власть стать соком жизни на Земле».Леонардо да Винчи
5 группа. «Вода, у тебя нет ни вкуса, ни цвета, ни запаха, тебя невозможно описать, тобойнаслаждаются, не ведая, что ты такое. Нельзя сказать, что ты необходима для жизни: ты — сама жизнь. Ты наполняешь нас радостью, которую не объяснить нашими чувствами».
Антуан де Сент-Экзюпери
В заключении фрагмент фильма о значении воды, растворов…
Я искренне верю, что вам сегодня было настолько же приятно работать, как и мне. Я благодарю вас за совместный труд, за вашу помощь. Всем спасибо за урок. Всего доброго.
Приложение 1
- Перед вами на столе находится коллекция дисперсных систем, мне бы хотелось чтобы вы, используя учебник на стр. 96-102, попытались классифицировать эти системы на группы, ответить на вопрос (работа в группах).
Консультанты являются помощниками и в конце работы оценивают каждого учащегося.
1-я группа: молоко, нефть, капельки жира в лимфе.
ВОПРОС:Дайте определение и приведите примеры эмульсий, которые человек применяет в практической деятельности?
Приложение 1
- Перед вами на столе находится коллекция дисперсных систем, мне бы хотелось чтобы вы, используя учебник на стр. 96-102, попытались классифицировать эти системы на группы, ответить на вопрос (работа в группах).
Консультанты являются помощниками и в конце работы оценивают каждого учащегося.
2- я группа: зубная паста, мази.
ВОПРОС:Дайте определение суспензий и назовите практически значимые строительные суспензии?
Приложение 1
- Перед вами на столе находится коллекция дисперсных систем, мне бы хотелось чтобы вы, используя учебник на стр. 96-102, попытались классифицировать эти системы на группы, ответить на вопрос (работа в группах).
Консультанты являются помощниками и в конце работы оценивают каждого учащегося.
3-я группа: гели для душа, почва, гели после бритья, кремы.
ВОПРОС:Чем определяется срок годности косметических и медицинских гелей?
Приложение 1
4-я группа.Как классифицируют дисперсные систем по агрегатному состоянию дисперсионной среды и дисперсной фазы? Приведите примеры, используя рис. 88 стр. 104(Слайд 9, 10, 11).
Приложение 2
Задача №1. Вычислить массовую долю растворенного вещества, если масса раствора 500 г, а масса соли 25 г.
Задача №2. В воде массой 40 г растворили 10 г сахара. Определить массовую долю раствора.
Задача №3. Для полоскания горла используют 4% раствор пищевой соды. Сколько понадобиться соды и воды, что бы приготовить раствор массой 200 г?
Задача №4. Рассчитать массу воды, которую необходимо добавить к раствору гидроксида калия массой 200 г с массовой долей растворенного вещества 12% для приготовления раствора с массовой долей 5% гидроксида калия? Ответ соли - 24 г, воды – 280 г
Приложение 3
1 группа.«Фармацевты» Заменителем крови является 0,9% раствор поваренной соли. Рассчитайте сколько необходимо взять соли и воды, для приготовления 200 г такого раствора?
Приложение 3
2 группа. «Лаборанты» На урок химии лаборанту для опытов необходимо приготовить раствор серной кислоты. Рассчитайте массу воды, которую необходимо добавить к раствору серной кислоты, массой 200 г с массовой долей вещества 70% для приготовления раствора с массовой долей 5%?
Приложение 3
3 группа.«Домохозяйки» Соление огурцов производят в 5%-ном растворе поваренной соли. Сколько соли и воды необходимо для приготовления 500 г такого раствора
Приложение 3
4 группа. «Строители» Чтобы построить современный долговечный дом − обойтись без раствора, практически, невозможно. Он нужен для устройства фундамента, полов, кладки стен, монтажа плит перекрытия, возведения камина и внутренней отделки помещений и фасада дома. Это далеко не полный перечень работ, где может применяться тот или иной вид строительного раствора.
Задача. Необходимо приготовить 15% известковый раствор массой 140 г, сколько вы возьмете воды и сколько оксида кальция для приготовления раствора?
Приложение 4






https://nsportal.ru/shkola/khimiya/library/2016/12/13/razrabotka-uroka-himii-na-temu-rastvory


 Приказ о проведении
Приказ о проведении
 Положение
Положение
 Выписка из Протокола
Выписка из Протокола
 Диплом победителя
Диплом победителя
 Диплом за инновационную деятельность
Диплом за инновационную деятельность
 Благодарность
Благодарность






















































Чтобы оставлять комментарии, вам необходимо авторизоваться на сайте. Если у вас еще нет учетной записи на нашем сайте, предлагаем зарегистрироваться. Это займет не более 5 минут.